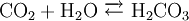Viele können gerade mal das Wort Kohlendioxid (CO2) schreiben und nach plappern, wie sich CO2 chemisch-physikalisch in Trinkwasser oder Meerwasser verhält.
In Abhängigkeit von Temperatur (t), Druck (p), ph-Wert und Salzgehalt, ausgedrückt über die el. Leitfähigkeit æ (mS/m) liegen folgende drei Gleichgewichte in der wässrigen Phase vor :
1.
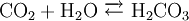
2.

3.

Als Trivialnamen für die Summe aus gelöstem Kohlendioxid und Kohlensäure ist „freie Kohlensäure“ gebräuchlich. Sie steht der Summe von Carbonat und Hydrogencarbonat als „gebundener Kohlensäure“ gegenüber.
Nur das gelöste Kohlendioxid kann in die Gasphase (Atmosphäre) übertreten.
Meerwasser hat einen ph-Wert von 7,8 - 8,2. Bei diesen pH-Werten beträgt der Anteil an CO2/H2CO3 gerade mal 1-2 % der ∑ CO2, das in die Atmosphäre gelangen kann.
Die ph-Wert abhängige Verteilung der CO2-Spezies für reines, salzfreies Wasser
Zitat von quer







 Mit Zitat antworten
Mit Zitat antworten